2021.07.19
国産セアカゴケグモ抗毒素製造と非臨床試験の詳細を山本明彦先生に記載いただきました。
国産セアカゴケグモ抗毒素製造と非臨床試験
山本 明彦 国立感染症研究所(感染研) 安全実験管理部
1.はじめに
セアカゴケグモ(Latrodectus hasseltii:図1)は、ヒメグモ科に分類される雌のみ有毒の小型のクモの一種である。和名は、「背中の赤いゴケグモ」の意味で東アジアからオーストラリア、南太平洋諸国まで広く分布する。日本国内には生息していなかったが、1995年9月に大阪府高石市、次いで三重県四日市市の埋立地で発見されて以降、生息地域を全国に拡大し2019年8月現在秋田県、青森県を除く全国に分布している(図2:参照1)特定外来生物である。攻撃性はないが、ヒトの生活環境の近くに生息し、側溝の内部、その金属製の蓋の隙間、宅地の水抜きパイプの内部、フェンスの基部、花壇のブロックの内部など巣を作る隙間があり、日当たりがよく、暖かく、餌となる昆虫のいる所に巣を作り繁殖し、触ると咬まれることがある。咬まれた直後は、軽い痛みを感じる程度だが、次第に痛みが増加し、腹痛、胸痛などが起こる場合がある。頻度はまれだが、重症になると、嘔吐、発熱、高血圧、頻脈などの神経毒による全身症状が現れる。原産地のオーストラリアでは、死亡例の報告もあり、重症例には抗毒素治療も行われている(参照2-4)。国内調査データのある大阪府内の咬症例は1995年から2019年までに96症例が公表されているが、2006年以降2013年ころまで大阪府内を中心に明らかに増加し、その後横ばい状況である(参照5)。
2.セアカゴケグモ抗毒素製造に至る経緯
国内でのセアカゴケグモ生息地の拡大と咬傷事例の増加は、幅広い年齢層での咬傷機会の拡大を示す。咬傷時に重症になった場合、全身症状と激しい痛みを伴う、また、外来の毒性生物が身近な環境に生息域を広げ、刺されると大変痛く重症例もあることから国民の不安が大きい。オーストラリアではCSL社の抗毒素が開発されてからセアカゴケグモ咬傷による死亡者は報告されていない事実も、治療に抗毒素製剤の必要性が高まる。この状況を受けて、2013年度に発足した厚生科学研究とAMED研究費「抗毒素の品質管理及び抗毒素を使用した治療法に関する研究」:一二三亨研究代表者(聖路加国際大学)では、臨床研究としてセアカゴケグモウマ抗毒素の輸入と国産ヤマカガシ抗毒素の使用時の副反応対策としての保証体制の整備、咬傷発生時のスムースな抗毒素輸送の検討と備蓄場所の検討等の検証・研究が行われた。
セアカゴケグモ咬傷への対策として、オーストラリアCSL社製セアカゴケグモウマ抗毒素を医師による個人輸入にて一定数購入し、咬傷事例が起きた場合はその治療薬として提供する計画であったが、実際の当該抗毒素の個人輸入は困難な状況であった。研究班としてそれぞれの希少疾病に対応してゆく中で、海外抗毒素製剤の個人輸入が著しく滞る状況があり、研究班の目的の1つであるセアカゴケグモ咬傷に対する国民の安全安心の確保を考慮すると、ヤマカガシ抗毒素の製造と同様に研究班において国内でのセアカゴケグモ抗毒素の製造の必要性が増してきた。2015年、セアカゴケグモについては、国産化セアカゴケグモ抗毒素の製造を実施することを決定した。国産化セアカゴケグモ抗毒素が完成した後には、安定的な供給ができるほか、アウトブレイクに対しても十分な対応が可能となると想定された。
3. 国産セアカゴケグモ抗毒素の製造へ準備
国内でのウマを用いた抗毒素製剤製造に必要な情報について、オーストラリアでセアカゴケグモ抗毒素製剤製造社のCSL社に分担研究者の㈶化学及血清療法研究所(化血研)を通じて情報提供を求めたが得られなかった。そこで、数少ない公知文献情報を参照した。1961年に発表された文献ではリン酸アルミニウムを混合した毒素を用いたウマ免疫によって抗体価上昇が報告された(参照6)。免疫計画やの品質管理試験を計画し、まずウサギを用いてセアカゴケグモ抗毒素試験免疫の検討を実施した。具体的には3種類の免疫方法を比較した。1)フォルマリン不活化毒素とオイルアジュバントの組み合わせ、2)無処置毒素とオイルアジュバントの組み合わせ、3)無処置毒素とリン酸アルミニウムアジュバントの組み合わせである。3種類の免疫方法で免疫したウサギから採血を行い、そのセアカゴケグモ毒素中和抗体価から免疫方法を評価した。
まず、免疫抗原の作成のためにセアカゴケグモ粗毒素を収集した。分担研究者である感染研の昆虫医科学部を通して大阪ペストコントロール協会および西宮市環境衛生課の協力の下、大阪府内で10,186頭、西宮市近郊で1,217頭の合計11,524頭の雌グモを捕獲した。昆虫医科学部においてそのうちの10,007雌を解剖し、個別に摘出した毒腺(図3)から毒素を抽出、粗精製を行い1ロット化した。一部の毒素を用いてタンパク量を定量したところ、1.5-2.5 mg/mlであった。最終的に1ロット化し、タンパク量約236 mgと推定された。総量170 mlの毒素粗精製物を得た。
捕獲精製した毒素液の一部を予備検討のためにウサギの免疫で用いるため免疫用抗原の調整として、フォルマリン不活化を実施した。免疫賦活のためのアジュバントとしては、オイルアジュバントとリン酸アルミニウムの2種類のアジュバントを用いて検討した。ウサギの免疫は、前述の3種類の免疫方法でそれぞれ2頭の背部皮下に投与し、セアカゴケグモ毒素に対する免疫ウサギの血清中の中和抗毒素価測定を行った。3種類の免疫方法の内フォルマリン不活化毒素とオイルアジュバントの組み合わせでの免疫が最も高い抗体価を得た。
4.セアカゴケグモ抗毒素の力価試験方法及びウマ免疫方法の検討
国産抗毒素の有効性を確認する方法としての力価試験法の検討を感染研免疫部にて実施した。国内で採取されたセアカゴケグモより抽出された粗毒の性状確認と抗毒素の力価試験確立を目的とした。セアカゴケグモ毒素のタンパク含有量を測定し、毒素の主成分であるα–ラトロトキシンの割合と安定性について常法にて確認した。次に、種々の毒素量をマウスに投与して、10日間生死を観察してLD50を算出した。さらに、40μgの毒素と種々に希釈した抗毒素を混和して1時間静置し、マウスに静脈内投与して10日間生死を観察して抗毒素の力価を測定した。その結果、毒素の主成分であるα–ラトロトキシンはどのロットでも良好の保存されており、室温または4℃での長期間の保管にも安定であることが判明した。毒素のLD50を算定した所、平均9.16899μgであった。確立した力価試験に基づき有効期限が過ぎた抗毒素の力価を測定した所、両者とも有効期限を過ぎても表示力価を維持していることが確認された。このようにして、セアカゴケグモ抗毒素に対する力価試験を確立した。また、毒素は長期間安定して毒性を維持することが判明した(参照7)。
さらに、化血研にてセアカゴケグモ抗毒素の製造のためウマ4頭を用いた免疫計画を作成した。ウサギでの基礎試験結果、及び化血研における抗毒素製剤製造実績を参考にし、アルミニウムアジュバントのセアカゴケグモ毒素吸着性能評価として、水酸化アルミニウム及びリン酸アルミニウムをそれぞれPHの異なる2条件で毒素の吸着量を検討した上で以下の4つの免疫方法を計画した。(1)毒素免疫法: 前述文献における免疫法を引用し、感染研での基礎試験結果を加味し、追加免疫回数は4回とした。なお、文献ではアジュバントとしてリン酸アルミニウムを使用していたが、事前検討においてリン酸アルミニウムよりも高い毒素吸着性能を示した水酸化アルミニウムを使用した。(2)トキソイド免疫法(定量追加免疫): 化血研における従来の抗毒素製造条件を参考として、基礎免疫回数はトキソイドで定量3回、免疫量は3mgと一定量に設定した。 (3)トキソイド免疫法(増量追加免疫): トキソイドによる増量追加免疫を追加した。(4)トキソイド・毒素混合免疫法: 毒素による増量追加免疫を検討することとした。毒素あるいはトキソイドにアジュバントとしてアルミニウムアジュバント又はオイルアジュバントを混合した4条件のウマ免疫計画を立案した(表1)。
5.乾燥セアカゴケグモウマ抗毒素の試作製造
1)ウマ免疫用のセアカゴケグモの捕獲とその毒素の粗精製、2)毒素を用いた力価試験方法の検討、3)ウサギによる予備試験を経て、4)ウマによる抗毒素製造のための免疫方法の検討が終了した。2000年の研究班による製造依頼と同様の手続きにて、AMED研究資金の援助により化血研のウマ抗毒素製造設備を用いて製造を開始した。国内採取セアカゴケグモ粗毒素(あるいはそのホルマリントキソイド)を抗原として健康馬に免疫し、毒素中和抗体価の比較的高い馬血漿から免疫グロブリン画分を精製し原液を得た。CSL社抗毒素と同様のsingle dose用(力価500 U/dose程度)の凍結乾燥条件を検討した上で、この原液(一部)を希釈して安定剤を添加後に凍結乾燥を行い、試作品を製造した。これらの原液ならびに試作品について、それぞれ既存抗毒素製剤を参考に参考規格を設定し、品質試験を実施した。力価試験は感染研免疫部の分担研究者によって行われた。力価試験以外の試験項目のうち既存蛇毒抗毒素において設定されている規格を参考規格として設定し、それぞれ生物学的製剤基準又は日本薬局方に準じて実施した。乾燥セアカゴケグモウマ抗毒素: 精製原液の一部を使って試作品(力価500U/dose)を約6,000本製造し、未使用の馬血漿及び精製原液は-80℃に凍結保存した。品質試験の結果、精製原液は迷入ウイルス否定試験ならびに設定した参考規格に適合し、試作品も参考規格に適合した(表2: 参照8)。
続いて、製造されたセアカゴケグモ抗毒素の中和抗体価測定を実施した。免疫法による中和抗体価の推移を表2に示す。ウマ基礎免疫後抗体価が上昇していることが確認された。このため、予定通り休止期間後追加免疫を複数の方法で実施した。免疫方法のうち、追加免疫で抗原を増量させていく方法が最も高い中和抗体価を得ることができた。また、製剤工程を経て、原液、小分け凍結乾燥品に十分な力価を維持していることが確認された。非臨床試験における製剤の安定性を評価するために、溶解後室温に6時間放置した後の力価を測定したが、6時間放置後においても力価の低下は認められなかった。4つの免疫方法の中ではトキソイド増量追加免疫法で最も高い中和抗体価が測定された。また、免疫終了後部分採血を行った場合、急速に血漿中抗体価が低下することが明らかになった。結果として、製剤化によっても十分な収量と力価が期待できる血漿を原材料としてセアカゴケグモ抗毒素の製品化が実施され、必要とされる力価を維持し、かつ安定な抗毒素小分け製品が確保された。2000年に製造したヤマカガシ抗毒素と比較するとそのタンパク含有量が1/3以下で、タンパク含量が少なく高活性の比活性の高い抗毒素製剤が製造された。セアカゴケグモ毒素という今まで経験のない抗原を用いて、しかも製造に関する情報が大変少ない中このような良質の製剤を製造できたのは、偏にウマ抗毒素製剤の製造経験が豊富な化血研の技術力によるものと考える。
6.GLP準拠の安全性試験の実施
製造されたセアカゴケグモ抗毒素について、GLP安全性試験を実施した。ヒトへの投与経験がない国産抗毒素を患者に初めて投与するには、少なくともGLP適合非臨床試験及び第I相試験相当の試験が必要との研究班内で議論を行った。国産抗毒素は、製造年度にnon-GLPの非臨床安全性試験は実施し、一定の安全性を確認したが、今後の健常人や患者への投与を考慮して、GLP試験の情報は有用との厚労省結核感染症課及びAMEDからの支持を得て、国産抗毒素のGLP試験を実施する方向となった。
ここで、GLP試験とは、過去の薬害事件の反省から、新規医薬品の開発において安全性を正しく評価するための試験適用基準として制定された。GLPは、ソフトとハードの両面から遵守すべき点を規定したものである。基本構成として、信頼性保証部門の設置、試験を外部施設に委託する場合の委託者の責務を明確にするとともに、試験施設の構造設備、標準操作手順書の作成、動物の管理、プロトコールや最終報告書の作成などが規定される。このようなGLP試験を実施できる各施設は、定期的にPMDAによる適合検査を受ける。
国産セアカゴケグモ抗毒素については、(株)新日本科学というGLP試験施設に依頼して実施した。まず具体的なGLP試験として必要な試験項目は以下の6項目の試験が計画された。I. 力価試験法の検討試験、II. 特性バリデーション試験: タンパク濃度、純度測定、力価試験等の測定法の妥当性の確認を含む試験、III. 特性安定性試験: 外観、pH、タンパク濃度、純度試験、力価試験、IV. 投与液安定性試験: 保存条件及び保存期間を担保、V. ウサギにおける筋肉局所刺激性試験、VI. ラットにおける間歇反復静脈内投与試験である。
- 力価試験法の検討として、予定されている乾燥セアカゴケグモウマ抗毒素の毒性試験(GLP準拠)において、乾燥セアカゴケグモウマ抗毒素の分析項目としてマウスを用いた力価試験法を行い、確立された力価試験法の妥当性が確認された。
- 特性試験法バリデーション試験として、乾燥セアカゴケグモウマ抗毒素の特性試験を実施するために、純度試験法(SE-HPLC法)、定量法(BCA法)及び力価試験法の妥当性を確認した。また、調製液中の乾燥セアカゴケグモウマ抗毒素の純度及び濃度測定を実施するために、紫外部検出によるHPLC法及びBCA法の妥当性を確認した。
III. 特性安定性試験: 外観、pH、タンパク濃度、純度試験、力価試験として、乾燥セアカゴケグモウマ抗毒素の特性試験[項目:性状(外観)、類縁物質及び純度(SE-HPLC法)、定量(BCA法)及び力価]を実施し、特性及び保存期間中の安定性を確認した。
- 投与液安定性試験として、PBSを媒体とした調製液中における乾燥セアカゴケグモウマ抗毒素の冷蔵24時間+室温2時間の安定性を確認した。
V.ウサギにおける筋肉局所刺激性試験として、乾燥セアカゴケグモウマ抗毒素を日本白色種雄ウサギの大腿部の外側広筋に1.0 mL/siteを2時間間隔で2回筋肉内投与し、投与後2及び14日に筋肉局所刺激性について調べた。観察期間中、全例で死亡はみられず、一般状態及び体重推移に異常はみられなかった。また、投与部位観察において、各群全例で紅斑/痂皮及び浮腫はみられなかった。
- ラットにおける間歇反復静脈内投与試験として、抗毒素製剤は血清病のリスクがあることから、本剤による血清病リスクの評価を主な目的として、本毒性検討を行った。ラット尾静脈に2週間間隔2回投与し、2回目投与後2および28日目に剖検を行い肉眼的観察し、評価した。検査項目として、剖検したラット全身組織の病理組織学的観察を実施した。観察期間中、全例で死亡はみられず、一般状態、体重、摂餌量、眼科的検査、尿検査、血液学的検査、血液生化学的検査、剖検、器官重量及び病理組織学的検査のいずれにおいても、被験物質に起因すると考えられる毒性変化はみられなかった。このように検討したIからVIまでのすべてのGLP準拠の安全性試験を実施した結果、今回製造した国産セアカゴケグモ抗毒素は、どの項目についても問題の無い結果となった(参照9)。
7.おわりに
環境省指定特定外来生物であり、国内で初めて発見されてから25,6年でほぼ全国にその生息域を広げたセアカゴケグモの咬傷重症例に対応するために、国産セアカゴケグモ抗毒素を製造し、GLP準拠の安全性試験を問題なく終了した。この国産抗毒素をヒトに使用するため、もう一つの条件として、第I相の臨床試験相当を実施し、その結果をもって、この薬剤を抗毒素班の臨床研究に使用可能となるところであったが、第I相の臨床試験は行われていない。本抗毒素は未承認薬品であり、ヒトへの投与にはその安全性試験が必須であると考慮しての試験計画ではあった。しかし、研究班が3年の区切りを経て代表者の交代を含めた研究内容の拡大もあり、また、この抗毒素の位置づけについて承認薬を目指す議論もあってヒトへの投与試験は行われていない。
本抗毒素は製造から3年が経過した。海外の抗毒素製剤と異なり、凍結乾燥製剤である国内製造ウマ抗毒素製剤の使用期限は安定で10年と規定されている。また、研究班の目的の一つであるヤマカガシ抗毒素は、製造後20年を経ているが、その品質に著しい劣化は起きていない。国産セアカゴケグモ抗毒素製剤も製造3年後の品質管理試験の結果は、その品質の劣化は見られていない。海外製品に比較しても十分な効力が期待できる国産抗毒素が大量に製造されていながら、一切その使用はなされていない。この抗毒素が国民に投与できる状態となって、供給の不安定な海外製品に頼らなくてよい状況ができることを期待するものである。現在まで、辛くも海外製品のセアカゴケグモ抗毒素製剤が輸入できて備蓄されている。また、セアカゴケグモによる咬傷自体は起きているが、幸いにして抗毒素を治療用に投与すべき重症例もこの間起きていない。しかし、海外からの抗毒素製剤の調達は決して安定的ではなく、使用期限が近づくたびに輸入先を探して綱渡りのような供給ができているに過ぎない。
セアカゴケグモ咬傷は著しい希少疾病であり、ヒトを用いた臨床試験は事実上不可能な本抗毒素製剤を承認薬として上梓するには、責任製造会社とその承認部署であるPMDA、厚生労働省の密接な協議が必要で、この点は現在も続く研究班の検討課題となっている。
図1 セアカゴケグモの雌
2014年度AMED報告書より
図2. 日本国内のセアカゴケグモ分布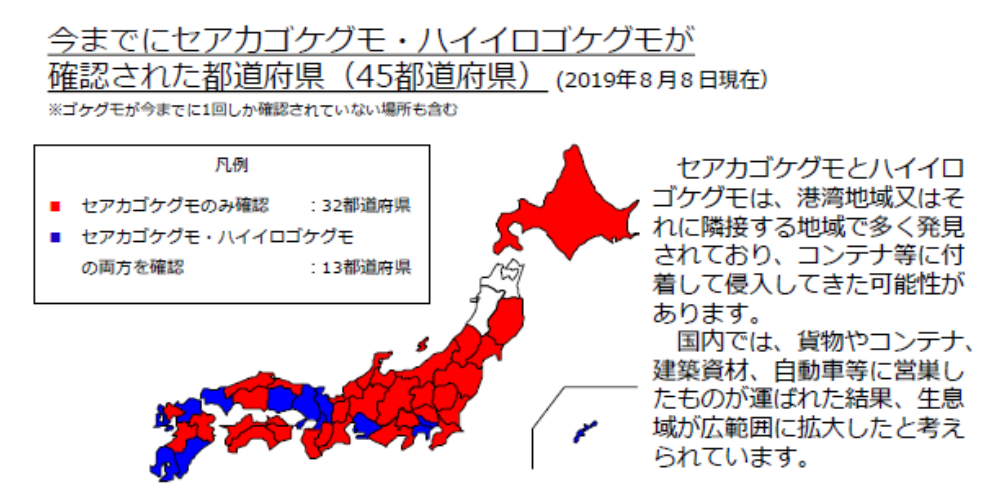
環境省ホームページより
図3. セアカゴケグモの毒腺(一対の茶色の牙に続く白色組織)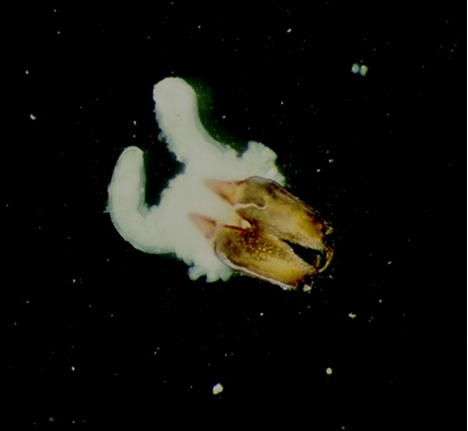
2014年度AMED報告書より
表1. セアカゴケグモ免疫用抗原のウマ免疫計画
No.1 毒素免疫法
|
|
基礎免疫(毒素) |
|
追加免疫(毒素) |
||||||||
|
免疫回数 |
1 |
2 |
3 |
4 |
5 |
6 |
|
1 |
2 |
3 |
4 |
|
免疫量(mg) |
0。01 |
0。05 |
0。1 |
0。3 |
0。8 |
2 |
|
1 |
2 |
3 |
6 |
|
アジュバント |
Al |
Al |
Al |
Al |
Al |
Al |
|
Al |
Al |
Al |
Al |
No.2 トキソイド免疫法(定量追加免疫)
|
|
基礎免疫(トキソイド) |
|
追加免疫(トキソイド) |
|||||||
|
免疫回数 |
1 |
2 |
3 |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
免疫量(mg) |
3 |
3 |
3 |
|
3 |
3 |
3 |
3 |
3 |
3 |
|
アジュバント |
FIA |
FIA |
FIA |
|
FIA |
FIA |
FIA |
FIA |
FIA |
FIA |
No.3 トキソイド免疫法(増量追加免疫)
|
|
基礎免疫(トキソイド) |
|
追加免疫(トキソイド) |
|||||||
|
免疫回数 |
1 |
2 |
3 |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
免疫量(mg) |
3 |
3 |
3 |
|
1 |
2 |
3 |
6 |
12 |
24 |
|
アジュバント |
FIA |
FIA |
FIA |
|
FIA |
FIA |
FIA |
FIA |
FIA |
- |
No.4 トキソイド・毒素混合免疫法
|
|
基礎免疫(トキソイド) |
|
追加免疫(毒素) |
|||||||
|
免疫回数 |
1 |
2 |
3 |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
免疫量(mg) |
3 |
3 |
3 |
|
1 |
2 |
3 |
6 |
12 |
24 |
|
アジュバント |
FIA |
FIA |
FIA |
|
FIA |
FIA |
FIA |
FIA |
FIA |
- |
2015年度AMED報告書より
図表
参照資料
- 昆虫情報処理研究会HP (https://www.insbase.ac/xoops2/modules/xpwiki/)
- Isbister GK, White J. Clinical consequences of spider bites: recent advances in our understanding. Toxicon. 43, 477-492, 2004.
- Kobayashi M. et al., Reactivity of an antivenom against the red-back spider, Latrodectus hasseltii, to venom proteins of two other spiders of Latrodectus introduced to Japan. Med. Entomol. Zool. 49, 351-355, 1998.
- Hifumi T. et al., A national survey examining recognition, demand for antivenom, and overall level of preparedness for redback spider bites in Japan. Acute Medicine & Surgery, 18, 310-314, 2016.
- https://www.pref.osaka.lg.jp/kankyoeisei/seaka/jiko.html
- Wiener, S., ‘Red Back Spider Antivenene’, The Medical Journal of Australia, 2, 41-44, 1961.
- Matsumura T. et al., Jpn. J. Infect. Dis., 71, 116–121, 2018
- Mori S. et al., Jpn. J. Infect. Dis., 70, 635–641, 2017
- Yamamoto A. et al., J. Toxicol. Pathol. 31, 105–112, 2018.